Fosfaat
Voorkoms
|
Algemeen | |
|---|---|
| Naam | Fosfaat |
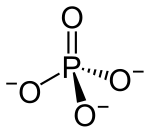 |

|
| Termochemiese radius | 2,30 Å [1] |
| 206,8 [Scm2/mol][2] | |
| Lys van anione | |
Fosfaat (PO43-) is die vorm waarin fosfor die meeste in verbindings voorkom. Fosfate is suurreste van fosforsuur (H3PO4). Die meeste fosfate los nie maklik in water op nie, en kan daarom maklik uit 'n oplossing met 'n neerslagreaksie verwyder word.
Fosfate is belangrike misstowwe. Hulle word hoofsaaklik as apatiet gemyn. Hidroksielapatiet is 'n biologies belangrike stof. Dit is byvoorbeeld deel van ons tande.
Die fosfaatioon is 'n sterk basis. In water vorm dit maklik die waterstoffosfaatioon HPO2−4
- HPO2−4 + H2O H3O+ + PO3−4 Ka3= 3,98×10−13 [pKa3 = 12,37]


