Glikolipied
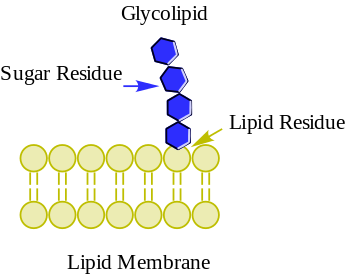
Glikolipiede is lipiede waaraan 'n koolhidraat deur 'n glikosidiese binding aangeheg is.[1] Hul rol is om die stabiliteit van die selmembraan in stand te hou, en sellulêre erkenning te fasiliteer, wat van kardinale belang in by die immuunreaksie en in die verbindings wat selle met mekaar maak om weefsels te vorm.[2] Glikolipiede kom op die oppervlak van alle eukariotiese selmembrane voor, waar hulle vanaf die fosfolipied dubbellaag in die ekstrasellulêre omgewing uitsteek.
Struktuur
[wysig | wysig bron]Die hoofkenmerk van 'n glikolipied is die teenwoordigheid van 'n monosakkaried of oligosakkaried wat gebonde is aan'n lipied. Die mees algemene lipiede in sellulêre membrane is gliserolipiede en sfingolipiede, wat onderskeidelik gliserol of sfingosien ruggrate het. Vetsure is gekoppel aan hierdie ruggraat, sodat die lipied as geheel 'n polêre kop en 'n nie-polêre stert het. Die lipied dubbellaag van die selmembraan bestaan uit twee lae van lipiede, waar die binneste en buitenste oppervlaktes van die membraan uit polêre kopgroepe opgemaak is, en die middelgedeelte van die membraan uit nie-polêre vetsuursterte.
Die sakkariede wat gekoppel is aan die polêre kopgroepe op die buitekant van die sel maak die ligandkomponente van glikolipiede uit, en is ook polêr, wat hulle toelaat om oplosbaar te wees in die waterige omgewing rondom die sel.[3] Die lipied en die sakkaried vorm 'n glikokonjugaat deur middel van 'n glikosidiese binding, wat 'n voorbeeld is van 'n kovalente binding. Die anomeriese koolstof van die suiker bind aan 'n vrye hidroksielgroep op die lipied ruggraat. Die struktuur van hierdie sakkariede wissel afhangende van die struktuur van die molekules wat aan hulle bind.
Metabolisme
[wysig | wysig bron]Glikosieltransferases
[wysig | wysig bron]Ensieme wat as glikosieltransferases bekend staan bind die sakkaried aan die lipiedmolekule, en speel ook 'n rol in die samestelling van die korrekte oligosakkaried, sodat die regte reseptor geaktiveer kan word op die sel wat reageer op die teenwoordigheid van die glikolipied op die seloppervlak. Die glikolipied word in die Golgi apparaat aanmekaar gesit, en word ingebed in die oppervlak van 'n vesikel wat dan vervoer word na die selmembraan. Die vesikel smelt saam met die selmembraan sodat die glikolipied gepresenteer kan word op die sel se buitenste oppervlak.[4]
Glikosiedhidrolases
[wysig | wysig bron]Glikosiedhidrolases kataliseer die af breek van glikosiedbindings. Hulle word gebruik om die oligosakkariedstruktuur van die koolhidraat te verander nadat dit op die lipied aangebring is. Hulle kan ook glikane van glikolipiede verwyder om hulle weer in ongemodifiseerde lipiede te verander.[5]
Gebreke in glikolipiedmetabolisme
[wysig | wysig bron]Die sfingolipidoses is 'n groep van siektes wat verband hou met die opbou van sfingolipiede wat nie korrek afgebreek is nie, gewoonlik as gevolg van 'n defek in 'n glikosiedhidrolase ensiem. Sfingolipidoses is tipies oorerflik, en die gevolge daarvan hang af van watter ensiem geraak is, en die graad van funksionele verlies. Een noemenswaardige voorbeeld is Niemann–Pick siekte wat pyn en skade aan neurale netwerke kan veroorsaak; dit is gewoonlik noodlottig in die vroeë kinderjare.[6]
Funksie
[wysig | wysig bron]Sel–sel Interaksies
[wysig | wysig bron]Die belangrikste funksie van glikolipiede in die liggaam is om te dien as erkenningsetels vir sel–sel interaksies. Die sakkariedgedeelte van die glikolipied bind aan 'n spesifieke komplementêre koolhidraat, of tot 'n lektien (koolhidraat-bindende proteïen) van 'n aangrensende sel. Die interaksie van hierdie seloppervlakmerkers is die basis van selerkenning, en inisieer sellulêre reaksies wat bydra tot aktiwiteite soos regulasie, groei, en apoptose.[7]
Immuunreaksies
[wysig | wysig bron]'n Voorbeeld van hoe glikolipiede binne die liggaam funksioneer is die interaksie tussen leukosiete en endoteelselle tydens inflammasie. Selektiene, 'n klas van lektiene wat op die oppervlak van leukosiete en endoteliale selle voorkom, bind aan die koolhidrate van glikolipiede om die immuunreaksie te inisieer. Hierdie binding veroorsaak dat leukosiete die sirkulasie verlaat en vergader naby die punt van inflammasie. Dit is die eerste bindingsmeganisme, wat gevolg word deur die uitdrukking van integriene wat sterker bande vorm en toelaat dat leukosiete migreer na die punt van inflammasie.[8] Glikolipiede is ook verantwoordelik vir ander reaksies, veral die erkenning van gasheer-selle deur virusse.[9]
Bloedgroepe
[wysig | wysig bron]Bloedgroepe is 'n voorbeeld van hoe glikolipiede op selmembrane sellulêre interaksies met die omliggende omgewing bemiddel. Die vier belangrikste menslike bloedgroepe (A, B, AB, en O) word bepaal deur die oligosakkaride wat gebind is aan 'n spesifieke glikolipied op die oppervlak van rooibloedselle, wat dien as 'n antigeen. Die ongemodifiseerde antigeen, bekend as die H antigeen, is die kenmerk van die tipe O, en is teenwoordig op die rooibloedselle van alle bloedgroepe. Bloedgroep A het 'n N-asetielgalaktosamien bygevoeg as die hoof bepalende struktuur; tipe B het 'n galaktose; en tipe AB het aldrie van hierdie antigene. Antigene wat nie teenwoordig is in 'n individu se bloed nie, sal veroorsaak dat teenliggaampies geproduseer word, wat aan die vreemde glikolipiede bind. Om hierdie rede kan mense met bloedgroep AB bloedoortappings van alle bloedgroepe ontvang (die universele akseptor), en mense met bloedgroep O kan as skenkers optree aan alle bloedgroepe (die universele skenker).[10]

Tipes glikolipiede
[wysig | wysig bron]- Gliseroglikolipiede: 'n subgroep van glikolipiede wat gekenmerk word deur 'n geasetileerde of nie-geasetileerde gliserol met ten minste een vetsuur as die lipiedkompleks. Gliseroglikolipiede is dikwels geassosieer met fotosintetiese membrane en hul funksies. Die subkategorieë van gliserolipiede afhang van die koolhidraat aangeheg.[11]
- Galaktolipiede: gedefinieer deur 'n galaktose suikereenheid wat gebind is aan 'n gliserol lipiedmolekule. Hulle kom in die chloroplastmembrane voor, en hou verband met fotosintetiese eienskappe.
- Sulfolipiede: 'n swael-bevattende funksionele groep in die suikergedeelte wat aan 'n lipied gebind is. 'n Belangrike groep is die sulfoquinovosiel diasielgliserole wat verband hou met die swawelsiklus in plante.[12]
- Glikosfingolipiede: 'n subgroep van glycolipiede wat gebaseer is op sfingolipied. Glikosfingolipiede is meestal geleë in die senuweeweefsel en is verantwoordelik vir die sellulêre seine.[13]
- Serebrosiede: 'n groep glikosfingolipiede wat betrokke is by senuwee selmembrane.[14]
- Galaktoserebrosiede: 'n tipe serebrosied met galaktose as die sakkariedgedeelte
- Glukoserebrosiede: 'n tipe serebrosied met glukose as die suikergedeelte; dikwels gevind in nie-neurale weefsel.
- Sulfatides: 'n klas van glikolipiede met 'n sulfaatgroep in die koolhidraat met 'n seramied lipied ruggraat. Hulle is betrokke by verskeie biologiese funksies vanaf immuunreaksies tot die senuweestelsel seinoordrag.
- Gangliosiede: die mees komplekse dier glikolipiede. Hulle bevat negatiefgelaaide oligosakkariede met een of meer siaalsuur residue; meer as 200[15] verskillende gangliosides is al geïdentifiseer. Hulle is mees volop in senuweeselle.
- Globosiede: glikosfingolipiede met meer as een suiker as deel van die koolhidraatkompleks. Hulle het 'n verskeidenheid van funksies; onvermoë om hierdie molekules af te breek lei tot Fabry siekte.
- Glikofosfosfingolipiede: komplekse glikofosfolipiede van swamme, giste en plante: in plante is hulle oorspronklik "fitoglikolipiede" genoem. Hulle mag wel net so 'n ingewikkelde stel van verbindings wees soos die negatief gelaaide gangliosiede in diere.
- Glikofosfatidielinositole: 'n subgroep van glikolipiede wat gedefinieer is deur 'n fosfatidielinositol lipiedgedeelte wat gebind is aan 'n koolhidraatkompleks. Hulle kan gebind word aan die C-eindpunt van 'n proteïen en het verskeie funksies wat verband hou met die verskillende proteïene waaraan hulle gebind word.[16]
- Serebrosiede: 'n groep glikosfingolipiede wat betrokke is by senuwee selmembrane.[14]
Verwysings
[wysig | wysig bron]- ↑ Voet, Donald; Voet, Judith; Pratt, Charlotte (2013). Fundamentals of Biochemistry Life at the Molecular Level (Fourth uitg.). Hoboken, NJ: John Wiley & Sons, Inc. ISBN 9781118129180.
- ↑ "Glycolipids". nature (in Engels). Nature Publishing Group. Geargiveer vanaf die oorspronklike op 19 Februarie 2017. Besoek op 1 November 2015.
- ↑ Aureli, Massimo; et al. (Augustus 2015). "Lipid Membrane domains in the Brain". BBA − Molecular and Cell Biology of Lipids. 1851 (8): 1006–1016. doi:10.1016/j.bbalip.2015.02.001. PMID 25677824.
- ↑ Williams, GJ; Thorson, JS (2009). "Natural product glycosyltransferases: properties and applications". Advances in Enzymology and Related Areas of Molecular Biology. 76: 55–119. doi:10.1002/9780470392881.ch2. PMID 18990828.
- ↑ Sinnott, M. L. "Catalytic mechanisms of enzymatic glycosyl transfer". Chem. Rev. 1990, 90, 1171–1202.[dooie skakel]
- ↑ Sandhoff, Kondrad (Desember 2015). "Sphingolipidoses". Journal of Clinical Pathology. 68 (12): 94–105. doi:10.1136/jcp.s3-8.1.94.
- ↑ Schnaar, Ronald (15 Junie 2004). "Glycolipid-mediated cell–cell recognition in inflammation and nerve regeneration". Archives of Biochemistry and Biophysics. 426 (2): 163–172. doi:10.1016/j.abb.2004.02.019. PMID 15158667.
- ↑ Cooper GM. The Cell: A Molecular Approach. 2nd edition. Sunderland (MA): Sinauer Associates; 2000. cell–cell Interactions. Available from: https://www.ncbi.nlm.nih.gov/books/NBK9851/
- ↑ Wang, Binghe; Boons, Geert-Jan (9 September 2011). Carbohydrate Recognition: Biological Problems, Methods, and Applications (in Engels). John Wiley & Sons. p. 66. ISBN 9781118017579.
- ↑ Erb IH (1 Mei 1940). "Blood Group Classifications, a Plea for Uniformity". Canadian Medical Association Journal. 42 (5): 418–21. PMC 537907. PMID 20321693.
- ↑ Neufeld, Elizabeth (Januarie 1964). "Formation of galactolipids". Biochemical and Biophysical Research Communications. 14 (6): 503–508. doi:10.1016/0006-291X(64)90259-1.
- ↑ Harwood, John L.; Nicholls, Rodney G. (1979). "The plant sulfolipid. A major component of the sulfur cycle". Biochemical Society Transactions. 7 (2): 440–7. doi:10.1042/bst0070440. PMID 428677.
- ↑ Hakomori, S (Desember 1995). "Functional role of glycosphingolipids in cell recognition and signaling". The Journal of Biochemistry. 118 (6): 1091–1103. PMID 8720120.
- ↑ Jurevics, H; Hostettler, J; Muse, ED; Sammond, DW; Matsushima, GK; Toews, AD; Morell, P (Mei 2001). "Cerebroside synthesis as a measure of the rate of remyelination following cuprizone-induced demyelination in brain". Journal of Neurochemistry. 77 (4): 1067–76. doi:10.1046/j.1471-4159.2001.00310.x. PMID 11359872.
- ↑ Role of ganglioside metabolism in the pathogenesis of Alzheimer's disease – a review-JOURNAL OF LIPID RESEARCH Volume: 49 Issue: 6 Pages: 1157–1175 Published: JUN 2008
- ↑ Paulick, Margot G.; Bertozzi, Carolyn R. (8 Julie 2008). "The Glycosylphosphatidylinositol Anchor: A Complex Membrane-Anchoring Structure for Proteins". Biochemistry. 47 (27): 6991–7000. doi:10.1021/bi8006324. ISSN 0006-2960. PMC 2663890. PMID 18557633.
