Oligosakkaried
'n Oligosakkaried (van die Grieks ὀλίγος olígos, "'n klein aantal", en σάκχαρ sácchar, "suiker") is 'n sakkariedpolimeer met 'n klein aantal (gewoonlik drie tot tien[1][2][3][4]) monosakkariede (eenvoudige suikers). Oligosakkariede kan baie funksies hê, insluitend selerkenning en selbinding. Glikolipiede, by voorbeeld, het 'n belangrike rol in die immuunreaksie.
Oligosakkariede is gewoonlik teenwoordig as glikane: oligosakkariedkettings wat gekoppel is aan lipiede of versoenbare aminosuur sykettings in proteïene, deur N- of O-glikosidiese bindings. N-gekoppelde oligosakkariede is altyd pentasakkariede wat aan asparagien gekoppel is deur 'n beta-skakel met die amien stikstof van die syketting.[5] O-gekoppelde oligosakkariede is normaalweg aan die hidroksielgroep van treonien of serien gebind. Nie alle natuurlike oligosakkariede kom as komponente van glikoproteïene of glycolipiede voor nie. Sommige, soos die raffinose reeks, stoor energie of vervoer kalsium in plante. Ander, soos maltodextriene of sellodekstriene, is die resultaat van mikrobiese afbraak van polisakkariede soos stysel of sellulose.
Glikosilering
[wysig | wysig bron]Glikosilering is die proses waar 'n koolhidraat kovalent aan 'n organiese molekuul gebind word, om strukture soos glikoproteïene en glycolipids te vorm.[6]
N-gekoppelde Oligosakkariede
[wysig | wysig bron]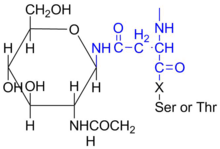
N-gekoppelde glikosilering behels die skakeling van 'n oligosakkaried aan asparagien deur 'n beta-koppeling met die amienstikstof van die syketting. Die proses van N-gekoppelde glikosilering vind kotranslationeel plaas: gelyktydig met die die proteïenvertaling, en help dus waarskynlik om die vou van die polipeptied te bepaal weens van die hidrofiliese aard van suikers. Alle N-gekoppelde oligosakkariede is pentasakkariede: vyf monosakkariede lank.
By N-glikosilering in eukariote, word die oligosakkariedsubstraat op die membraan van die endoplasmatic retikulum saamgestel.[7] By prokariote, vind hierdie proses vind by die plasmamembraan plaas. In beide gevalle is die akseptorsubstraat 'n asparagienresidu. Die asparagineresidu wat gekoppel word aan 'n N-gekoppelde oligosakkaried kom gewoonlik in die volgorde Asn-X-Ser/Thr voor, waar X enige aminosuur kan wees behalwe vir prolien, maar dit is skaars om Asp, Glu, Leu, of Tvp in hierdie posisie te sien.
O-gekoppel Oligosakkariede
[wysig | wysig bron]
Oligosakkariede wat deelneem in O-gekoppelde glikosilering word aan treonien of serien se hidroksielgroep gekoppel. O-gekoppelde glikosilering vind in die golgi apparaat plaas, waar monosakkariedeenhede tot 'n volledige polypeptiedketting toegevoeg word. Sel-oppervlak proteïene en ekstrasellulêre proteïene word O-glikosileer.[8] Glikosileringsetels in O-gekoppelde oligosakkariede word bepaal deur die sekondêre en tersiêre strukture van die polipeptied, wat bepaal waar glicosieltransferases suikers aanheg.
Geglikosileerde biomolekules
[wysig | wysig bron]Glikoproteïene en glikolipiede is per definisie kovalent gebind aan koolhidrate. Hulle is baie volop op die oppervlak van die sel, en hul interaksies dra by tot die algehele stabiliteit van die sel.
Glikoproteïene
[wysig | wysig bron]Glikoproteïene het verskillende oligosakkariedstrukture wat 'n beduidende uitwerking op baie van hul eienskappe het,[9] en daardeur die kritieke funksies soos antigenisiteit, oplosbaarheid, en weerstand teen proteases bepaal. Glikoproteïene tree byvoorbeeld as reseptore op die seloppervlak, as sel-adhesiemolekules, as immunoglobuliene, en as tumor antigene op.[10]
Glikolipiede
[wysig | wysig bron]Glikolipiede is belangrik by selerkenning asook vir modulering van die funksie van die membraanproteïene wat optree as reseptore.[11] Glikolipiede is lipiedmolekules wat gebind is aan oligosakkariede, oor die algemeen teenwoordig in die lipied dubbellaagvesikal. Daarbenewens kan hulle dien as reseptore vir sellulêre erkenning en seintransduksie. Die kopgedeelte van die oligosakkaried dien as'n bindingsvennoot by reseptoraktiwiteit. Die bindingsmeganismes van die reseptore aan die oligosakkariede hang af van die samestelling van die oligosakkariede wat blootgestel is bo die oppervlak van die selmembraan. Daar is 'n groot verskeidenheid in die bindingsmeganismes van glikolipiede, wat hulle so 'n belangrike teiken vir patogene as 'n terrein vir interaksie en toegang maak.[12] byvoorbeeld, die chaperone aktiwiteit van glikolipiede word bestudeer vir sy relevansie by MIV-infeksie.
Funksies
[wysig | wysig bron]Selerkenning
[wysig | wysig bron]Alle selle is bedek in glikoproteïene of glikolipiede, wat beide help om seltipes te bepaal. Lektiene, of proteïene wat koolhidrate bind, kan spesifieke oligosakkariede herken, en verskaf daardeur nuttige inligting vir selerkenning gebaseer op oligosakkariedbinding.
'n Belangrike voorbeeld van oligosakkaried selerkenning is die rol van glikolipiede by die bepaling van bloedgroepe. Die verskillende bloedgroepe word onderskei deur die koolhidraatverandering op die oppervlak van die bloedselle.[13] Dit kan gevisualiseer word met behulp van massaspektrometrie. Die oligosakkariede op die A, B en H antigene kom op die nie-reduserende punte van die oligosakkariedkettings voor. Die H antigeen (wat dui op 'n O bloedgroep) dien as 'n voorloper vir die A-en B-antigeen. Dus sal 'n persoon met bloedgroep B die A antigeen en H antigeen op die glikolipiede van die rooi bloedsel plasmamembraan hê. 'n Persoon met bloedgroep B het die B en H antigene. 'n Persoon met AB bloedgroep sal A, B, en H antigene teenwoordig. 'n Persoon met O bloedgroep sal slegs die H antigeen hê. Dit beteken dat alle bloedgroepe die H antigeen het, wat verduidelik hoekom die O bloedgroep bekend staan as die "universele skenker".
Sel Adhesie
[wysig | wysig bron]Baie selle produseer spesifieke koolhidraat-bindende proteïene wat bekend staan as lektiene, en wat sel adhesie deur oligosakkariede bemiddel.[14] Selektiene - 'n familie van lektiene - bemiddel sekere sel-sel adhesie prosesse, insluitend dié van leukosiete aan endoteelselle. By 'n immuunreaksie, kan endoteelselle sekere selektiene tydelik in reaksie op skade of besering uitdruk. In reaksie daarop, vind 'n wedersydse selektien-oligosakkaried interaksie plaas tussen die twee molekules wat die witbloedsel help om die infeksie of skade te elimineer. Proteïen-koolhidraatbinding word dikwels bemiddel deur waterstofbinding en van der Waalskragte.
Rol in die moeder-na-kind-oordrag van MIV-1
[wysig | wysig bron]Gemengde voeding van borsmelk en formule of ander nie-menslike melk, verhoog die risiko van nageboorte-oordrag van MIV-1.[15] die Meeste babas wat uitsluitlik borsgevoed word, kry nie die virus van die besmette moeder nie. Die spesifieke glikane wat teenwoordig is in borsmelk kan MIV-1-oordrag inhibeer deur mededinging met die MIV-1 oppervlakglikoproteïn gp120 vir binding aan dendritiese ICAM3-grypende nie-integrien (DC-SIGN). Menslike melk bevat baie komplekse oligosakkariede wat verskeie Lewis antigeen glikane dra. Hierdie menslike melk oligosakkariede verminder gp120 binding deur meer as 80%, en inhibeer sodoende die moeder-na-kind-oordrag van MIV-1.
Oligosakkariede in die dieet
[wysig | wysig bron]Frukto-oligosakkariede (FOS), wat in baie plantweefsel voorkom, is kort kettings van fruktose molekules. Hulle verskil van inulien, wat 'n veel hoër graad van polimerisasie as FOS het, en dus as 'n polisakkaried beskou word, maar soos inulien, word FOS beskou as oplosbare dieetvesel. Galaktooligosakkariede (GOS), wat ook natuurlik voorkom, bestaan uit kort kettings van galaktose. Hierdie verbindings kan nie in die menslike dunderm verteer word nie, en beweeg deur na die dikderm, waar hulle die groei van Bifidobacteria bevorder, wat voordelig is vir dermgesondheid.[16]
Mannan oligosakkariede (MOS) vind wye toepassing in veevoer om dermgesondheid te bevorder. Hulle word gewoonlik verkry uit die selwande van Saccharomyces cerevisiae gis. Mannan oligosakkariede verskil van ander oligosakkariede deurdat hulle nie fermenteerbaar is nie, en hul primêre voordeel is die agglutinering van tipe-1 fimbria patogene en immunomodulering.[17]
Bronne
[wysig | wysig bron]Oligosakkariede is 'n komponent van vesel in plantweefsel. FOS en inulien is teenwoordig in Jerusalem artisjok, klitskruid, sigorei, preie, uie, en aspersies. Inulien is 'n belangrike deel van die daaglikse dieet van die meeste van die wêreld se bevolking. FOS kan ook gesintetiseer word deur inwerking van die ensieme van die swam Aspergillus niger op sukrose. GOS kom natuurlik in sojabone voor, en kan gesintetiseer word uit laktose. FOS, GOS en inulien word ook verkoop as dieetaanvullings.
Verwysings
[wysig | wysig bron]- ↑ Sjabloon:MeshName
- ↑ Dairy Science and Technology, second edition. P. Walstra, J.T.M. Wouters and T.J. Geurts. CRC, Taylor & Francis, 2008
- ↑ Understanding Nutrition, Eleventh Edition. E. Whitney, S. R. Rolfes. Thomson Wadsworth, 2008
- ↑ http://www.britannica.com/EBchecked/topic/427621/oligosaccharide
- ↑ Voet, Donald; Voet, Judith; Pratt, Charlotte (2013). Fundamentals of Biochemistry: Life at the Molecular Level (4th ed.). Hoboken, NJ: John Wiley & Sons, Inc. ISBN 978-0470-54784-7.
- ↑ Essentials of Glycobiology. Ajit Varki (ed.) (2nd ed.). Cold Spring Harbor Laboratories Press. ISBN 978-0-87969-770-9.
- ↑ F. Schwarz, M. Aebi. Mechanisms and principles of N-linked protein glycosylation. Curr. Opin. Struct. Biol., 21 (2011), pp. 576–582
- ↑ Peter-Katalinic J. Methods in Enzymology: O-glycosylation of proteins. Methods Enzymol. 2005;405:139–171.
- ↑ Goochee C.F. 1992. Bioprocess factors affecting glycoprotein oligosaccharide structure. Dev. Biol. Stand. 76: 95–104.Review.
- ↑ Elbein AD. The role of N-linked oligosaccharides in glycoprotein function. Trends Biotechnol. 1991;9:346–52. doi: 10.1016/0167-7799(91)90117-Z.
- ↑ Moutusi Manna, Tomasz Róg, Ilpo Vattulainen. The challenges of understanding glycolipid functions: an open outlook based on molecular simulations. Biochim. Biophys. Acta, 1841 (2014), pp. 1130–1145
- ↑ Fantini J (2007) Interaction of proteins with lipid rafts through glycolipid-binding domains: biochemical background and potential therapeutic applications. Curr Med Chem 14: 2911–2917.
- ↑ Kailemia M.J., Ruhaak L.R., Lebrilla C.B., Amster I.J. Oligosaccharide analysis by mass spectrometry: a review of recent developments. Anal. Chem. 2014;86:196–212.
- ↑ Feizi, Ten (1993-10-01). "Oligosaccharides that mediate mammalian cell-cell adhesion". Current Opinion in Structural Biology 3 (5): 701–710. doi:10.1016/0959-440X(93)90053-N.
- ↑ Becquet, Renaud, et al. "Early mixed feeding and breastfeeding beyond 6 months increase the risk of postnatal HIV transmission: ANRS 1201/1202 Ditrame Plus, Abidjan, Cote d'Ivoire." Preventive medicine 47.1 (2008): 27-33..
- ↑ Moise, Ana Maria R. (31 Oktober 2017). The Gut Microbiome: Exploring the Connection between Microbes, Diet, and Health (in Engels). ABC-CLIO. p. 58. ISBN 9781440842658.
- ↑ rishi (Oktober 2003). In vitro fermentation characteristics of selected oligosaccharides by swine fecal microflora (Abstract (free)). URL besoek op 30 Maart 2013.
