Imidasool
|
Algemeen | |
|---|---|
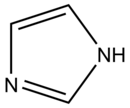
| Naam | Imidasool |
| IUSTC-naam | 1,3-diasa-2,4-siklopentadieen |
 |
 |
| Chemiese formule | C3H4N2 |
| Molêre massa | 68,08 g/mol |
| CAS-nommer | 288-32-4[1] |
| Voorkoms | Vastestof |
| Fasegedrag | |
| Smeltpunt | 90 °C |
| Kookpunt | 256 °C |
| Digtheid | 1,23 g/cm3, solied |
| Oplosbaarheid | opl. in koue water |
|
Suur-basis eienskappe | |
| pKa | 6,95 (vir die gekonjugeerde suur)[2] |
|
Veiligheid | |
| Flitspunt | 145 °C |
| LD50 | 220 mg/kg (rot; oraal, akuut) |
|
Tensy anders vermeld is alle data vir standaardtemperatuur en -druk toestande. | |
| Portaal | |

Die naam Imidasool is in 1887 geskep deur die Duitse chemikus Arthur Rudolf Hantzsch (1857–1935).[3] Imidasool is 'n heterosikliese aromatiese verbinding met die chemiese formule C3H4N2. Dit word geklassifiseer as 'n diasool en het nie-aangrensende stikstofatome.
Imidasool is 'n wit of kleurlose vaste stof wat in water oplosbaar is en het matige basiese eienskappe. Die stof word soms in die pH-gebied van 6,2-7,8 as buffer gebruik.
Baie natuurlike produkte, veral alkaloïede, bevat die imidasoolring. Hierdie imidasole deel die 1,3-C3N2-ring, maar het verskillende substituente. Hierdie ringstelsel is teenwoordig in belangrike biologiese boustene, soos histidien en die verwante hormoon histamien. Baie medisyne bevat 'n imidasoolring, soos sekere swamdodende middels, die stikstof-imidasool-reeks antibiotika en die kalmeermiddel "midazolam".[4][5][6][7][8]
As dit met 'n pirimidienring versmelt word vorm dit 'n purien, wat die mees natuurlik voorkomend stikstofbevattende heterosiklus is.[9]
Struktuur en eienskappe
[wysig | wysig bron]Imidasool is 'n eenvlakkige, 5-ledige ring. Dit bestaan uit twee ekwivalente tautomeriese vorme, omdat waterstof aan die een of die ander stikstofatoom gebind kan word. Imidasool is 'n sterk polêre verbinding, soos blyk uit sy elektriese dipoolmoment van 3,67 D.[10] Dit is baie oplosbaar in water. Die verbinding word as aromaties geklassifiseer vanweë die teenwoordigheid van 'n vlak ring wat 6 π-elektrone bevat ('n paar elektrone van die geprotoneerde stikstofatoom en een uit elk van die oorblywende vier atome van die ring). Hier volg 'n paar resonansiestrukture van imidasool:

Imidasool is amfoteries. Dit wil sê, dit kan funksioneer as 'n suur en as 'n basis. As suur is die pKa van imidasool 14,5, wat dit minder suur maak as Karboksielsure, fenole en imiede, maar effens meer suur as alkohole. Die suurproton is die een wat aan stikstof gebind is. Deprotonasie gee die imidasool-anioon, wat simmetries is.
As 'n basis is die pKa van die gekonjugeerde suur (aangehaal as pKBH+ om verwarring tussen die twee te voorkom) ongeveer 7, wat imidasool ongeveer sestig keer meer basies maak as piridien. Die basiese gedeelte is die stikstof met die alleenpaar (en nie gebonde aan waterstof nie). Protonasie gee die imidasolium-katioon, wat ook simmetries is.
Toepassings
[wysig | wysig bron]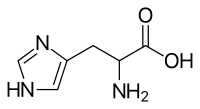
Imidasool vind ook biochemiese aanwending in geïmmobiliseerde metaalioonaffiniteitschromatografie (IMAC), 'n chromatografie-tipe wat gebruik word vir die suiwering van proteïene wat met die aminosuur histidien gemerk is. In IMAC veranker hierdie groep die proteïen op die nikkelatome van die chromatografiese kolom. 'n Oplossing van imidasool word gebruik om die proteïen van die kolom los te spoel.[11]
| Wikimedia Commons bevat media in verband met Imidasool. |
Verwysings
[wysig | wysig bron]- ↑ "Materiaalveiligheidsdatablad - Imidasool". sciencelab.com (in Engels). Geargiveer vanaf die oorspronklike op 4 April 2016. Besoek op 10 Januarie 2020.
- ↑ Walba, H. (1961). "Suurkonstante van arylimidazole en die se katione". J. Org. Chem. (in Engels). 26 (8): 2789–2791. doi:10.1021/jo01066a039.
{{cite journal}}: Onbekende parameter|coauthors=geïgnoreer (hulp) - ↑ Verslae van die Duitse Chemiese Vereniging. uit.20 (1887), bl.2267-3568. (Duits). HathiTrust (8 Oktober 2018). URL besoek op 10 Januarie 2020.
Justus Liebig se Annale van chemie. uit.249(1888). (Duits). HathiTrust (11 Oktober 2018). URL besoek op 10 Januarie 2020.
aanhaling: "Hantzsch het 'n hervorming van die nomenklatuur van asoolverbindings voorgestel, met 'n voorstel om die heterosikliese ring C3H3(NH)N "imidasool" te noem" - ↑ Karitzky, A. R. (1984). Omvattende Heterosikliese Chemie (in Engels). Vol. 5. pp. 469–498. ISBN 978-0-08-042072-1.
- ↑ Grimmett, M. Ross (1997). Imidasool- and Bensimidasool-sintese (in Engels). Academic Press. ISBN 978-0-08-053445-9.
- ↑ Pozharskii, A. F. (1997). Heterosikluse In die lewe en die samelewing (in Engels). John Wiley & Sons. ISBN 978-0-471-96033-1.
- ↑ Brown, E. G. (1998). Stikstofringe en sleutel biomolekule (in Engels). Kluwer Academic Press. ISBN 978-94-011-4906-8.
- ↑ Gilchrist, T. L. (1985). Heterosikliese Chemie (in Engels). Bath Press. ISBN 978-0-582-01421-3.
- ↑ Rosemeyer, H. (2004). "Die chemodiversiteit van purien as 'n bestanddeel van natuurlike produkte". Chemistry & Biodiversity (in Engels). 1 (3): 361–401. doi:10.1002/cbdv.200490033. PMID 17191854.
- ↑ Christen, Dines; Griffiths, John H.; Sheridan, John (1981). "Die mikrogolfspektrum van imidasool; Volledige struktuur en die elektronverspreiding van kernkwadrupoolkoppelingstensors en Dipoolmomentorientering". Zeitschrift für Naturforschung A (in Engels). 36 (12): 1378–1385. Bibcode:1981ZNatA..36.1378C. doi:10.1515/zna-1981-1220.
- ↑ "Imidasool - CAS 288-32-4". Santa Cruz biotechnology (in Engels). Geargiveer vanaf die oorspronklike op 8 September 2017. Besoek op 10 Januarie 2020.
