Inositol
|
Algemeen | |
|---|---|
| Naam | Inositol |
| IUSTC-naam | (1R,2R,3S,4S,5R,6S)-sikloheksaan-1,2,3,4,5,6-heksol |
 |
 |
| Chemiese formule | C6H12O6 |
| Molêre massa | 180.16 g/mol |
| CAS-nommer | 87-89-8 |
| Voorkoms | Wit poeier |
| Fasegedrag | |
| Smeltpunt | 225 - 227 °C |
| Kookpunt | |
| Digtheid | 1.752 g/cm3 |
| Oplosbaarheid | |
|
Suur-basis eienskappe | |
| pKa | |
|
Veiligheid | |
| Flitspunt | 143 °C |
|
Tensy anders vermeld is alle data vir standaardtemperatuur en -druk toestande. | |
| Portaal | |
Inositol of siklohexaan-1,2,3,4,5,6-hexol is 'n chemiese verbinding met die formule C6H12O6 oftewel (-CHOH-)6. Dit is 'n afgeleide van Sikloheksaan met ses hidroksielgroepe, wat dit 'n poliol maak, oftewel 'n veelvuldige alkohol. Dit kan in nege moontlike stereoisomere voorkom, waarvan cis-1,2,3,5-trans-4,6-siklohexaanhexol, of mio-inositol (voorheen bekend as meso-inositol of i-inositol), die mees algemene vorm in die natuur is.[1][2] Inositol is 'n suikeralkohol met die helfte van die soetheid van sukrose (tafel suiker).
Mio-inositol speel 'n belangrike rol as die strukturele basis vir 'n aantal sekondêre boodskappers in eukariotiese selle: die verskillende inositolfosfate. Daarbenewens speel inositol 'n belangrike rol as 'n komponent van die strukturele lipiede fosfatidielinositol (PI) en sy verskeie fosfate, die fosfatidielinositolfosfaat (PIP) lipiede.
Inositol of sy fosfate en gepaardgaande lipiede kom in baie kosse voor, veral vrugte soos spanspek en lemoene.[3] In plante dien die heksafosfaatvorm van inositol, fytiensuur of sy soute, die fitate, as fosfaatreserwe in sade, byvoorbeeld in neute en bone.[4] Fytiensuur kom ook voor in graan met hoë semelinhoud. Fytiensuur is egter nie direk biobeskikbaar vir die mens nie. Sommige voedselvoorbereidingstegnieke breek fitate af om dit verteerbaar te maak. Wanneer inositol egter in die vorm van gliserofosfolipiede voorkom, soos byvoorbeeld in lesitien, word dit goed geabsorbeer en is dit relatief biobeskikbaar.
Mio-inositol (sonder fosfaat) is voorheen beskou as 'n lid van die vitamien B - kompleks, sogenaamde Vitamien B8 in hierdie konteks. Aangesien dit deur die menslike liggaam vanaf glukose geproduseer word, is dit nie 'n essensiële voedingstof nie.[5]
Isomere en struktuur
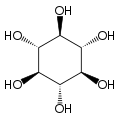
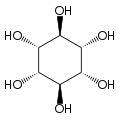
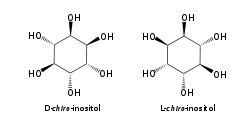
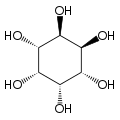
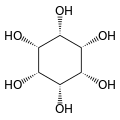
[wysig | wysig bron]Die isomeer mio-inositol is 'n meso-verbinding, en dus opties onaktief, want dit het 'n vlak van simmetrie. Daarom was meso-inositol 'n historiese naam vir hierdie verbinding. Behalwe mio-inositol, kom vier ander stereoisomere natuurlik voor, naamlik scyllo-, muco-, D-chiro-, en neo-inositol, alhoewel in minimale hoeveelhede. Die ander moontlike isomere, L-chiro-, allo-, epi-, en cis-inositol kom nie in die natuur voor nie. Soos hulle name aandui, is L- en D-chiro inositol die enigste paar enantiomere onder die stereoisomere van inositol.[6]

|
|
|
|
| mio- | scyllo- | muco- | chiro- |

|
|

|
 |
| neo- | allo- | epi- | cis- |
In sy mees stabiele konformasie, neem die mio-inositol isomeer die stoelkonformasie aan, wat die maksimum aantal van hidroksielgroepe na die ekwatoriale posisie skuif, waar hulle so ver moontlik vanmekaar is. In hierdie konformasie, het die natuurlike mio isomeer 'n struktuur waar vyf van die ses hidroksielgroepe (die eerste, derde, vierde, vyfde en sesde) ekwatoriaal is, terwyl die tweede hidroksielgroep aksiaal is.[7]
Biosintese
[wysig | wysig bron]Mio-inositol word uit glukose-6-fosfaat (G-6-P) in twee stappe gesintetiseer. Eerstens word G-6-P deur 'n inositol-3-fosfaatsintase ensiem geisomeriseer om mio-inositol 1-fosfaat te vorm, wat dan deur 'n inositol monofosfatase ensiem gedefosforileer word om vrye mio-inositol te vorm. In die mens word die meeste inositol in die niere gesintetiseer, tipies 'n paar gram per dag.[8]
Funksie
[wysig | wysig bron]Inositol, fosfatidielinositol en 'n paar van hulle mono- en polifosfate tree as sekondêre boodskappers op in 'n aantal intrasellulêre seintransduksiewëe. Hulle is by 'n aantal biologiese prosesse betrokke, insluitend:
- Insulien seintransduksie[9]
- Sitoskelet produksie
- Senuwee gleiding (epsien)
- Intrasellulêre kalsium (Ca2+) konsentrasiebeheer[10]
- Instandhouding van selmembraan potensiaal[11]
- Afbreek van vette [12]
- Geen-uitdrukking[13][14]
In een van die belangrike familie van seintransduksiewëe, word fosfatidielinositol 4,5-bisfosfaat (PIP2) in sellulêre membrane gestoor totdat dit deur enige van 'n aantal die seinproteïene vrygestel word en in verskeie tweede boodskappers omskep word, byvoorbeeld diasielgliserol en inositol trifosfaat.[15]
Fitiensuur in plante
[wysig | wysig bron]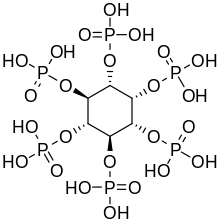
Inositolheksafosfaate, ook fitiensuur of IP6 genoem, is die belangrikste bergingsvorm van fosfor in baie plantweefsels, veral semels en sade.[16] Fosfor en inositol in fitaatvorm is oor die algemeen nie biobeskikbaar vir diere behalwe herkouers, omdat diere nie die spysverteringstelsel ensiem phytase besit wat nodig is om die fosfaat groepe te verwyder nie. Herkouers kan fitaat verteer, aangesien die ensiem fitase deur die rumen mikro-organismes geproduseer word.[17] Fitiensuur form ook chelate met belangrike minerale soos kalsium, magnesium, yster en sink, en maak hulle só onabsorbeerbaar, en dra by tot mineraaltekorte in mense wie se dieet afhanklik is van semels en saad vir hulle mineraalinname, soos in baie ontwikkelende lande.[18][19]
Inositol penta- (IP5), tetra- (IP4), en trifosfaat (IP3) word ook fitate genoem.
Gebruik in plofstofvervaardiging
[wysig | wysig bron]By die 1936 vergadering van die American Chemical Society, het professor Edward Bartow van die Universiteit van Iowa 'n kommersieel lewensvatbare metode voorgestel waardeur groot hoeveelhede van inositol uit die fitiensuur herwin kon word wat natuurlik teenwoordig is koringafval. As 'n moontlike gebruik vir die stof, het hy inositol nitraat voorgestel as 'n meer stabiele alternatief tot nitrogliserien.[20] Vandag word inositolnitraat gebruik om nitrosellulose te gelatiniseer, en word dus in baie moderne plofstowwe en vaste vuurpyl dryfmiddels gebruik.[21]
Navorsing en kliniese toepassings
[wysig | wysig bron]Groot dosisse van inositol is al bestudeer om depressie te behandel, maar onvoldoende bewyse bestaan vir die doeltreffendheid van hierdie behandeling.[22]
Inositol is effektief in die bestuur van vroeggebore babas wat aan 'n risiko vir infantiele respiratoriese nood sindroom blootgestel is, of as 'n behandeling vir die toestand.[23]
Inositol word beskou as 'n veilige en doeltreffende behandeling vir polisistiese eierstoksindroom (PCOS). Dit werk deur insuliensensitiwiteit te verhoog, wat help om eierstokfunksie te verhoog, en hiperandrogenisme te vermy.[24] Dit verminder ook die risiko van metaboliese siekte in mense met PCOS.[25]
Verdunningsmiddel vir dwelms
[wysig | wysig bron]Inositol word gebruik as 'n verdunningsmiddel vir baie onwettige dwelms soos kokaïen, metamfetamien, en soms heroïen,[26] waarskynlik as gevolg van sy oplosbaarheid, poeieragtige tekstuur, en laer soetheid (50%) in vergelyking met die meer algemene suikers.
Inositol woord ook in televisie en rolprente gebruik om kokaïen voor te stel.[27]
Voedingsbronne
[wysig | wysig bron]Mio-inositol is natuurlik teenwoordig in 'n verskeidenheid van voedsel, hoewel tabelle van voedselsamestellings nie altyd onderskei tussen lesitien, die biobeskikbare vorm, en die onbeskikbare fitaat vorm in graan.[28] Voedsel met die hoogste konsentrasies van mio-inositol (insluitende sy verbindings) sluit in vrugte, bone, graan en neute. Bone en graan bevat egter groot hoeveelhede van fitaat.
Verwysings
[wysig | wysig bron]- ↑ Synonyms in PubChem
- ↑ Synonyms in Commonchemistry.org
- ↑ "Myo-inositol content of common foods: development of a high-myo-inositol diet". The American Journal of Clinical Nutrition. 33 (9): 1954–67. 1980.
- ↑ http://www.phytochemicals.info/phytochemicals/phytic-acid.php.
- ↑ Reynolds, James E. F. (1 Januarie 1993). Martindale: The Extra Pharmacopoeia. Pennsylvania: Rittenhouse Book Distributors. p. 1379. ISBN 0-85369-300-5.
An isomer of glucose that has traditionally been considered to be a B vitamin although it has an uncertain status as a vitamin and a deficiency syndrome has not been identified in man
- ↑ Majumder, A. Lahiri (3 Oktober 2006). Biology of Inositols and Phosphoinositides (in Engels). Springer Science & Business Media. ISBN 9780387276007.
- ↑ Brady, Scott; Siegel, George; Albers, R. Wayne; Price, Donald (11 November 2005). Basic Neurochemistry: Molecular, Cellular and Medical Aspects (in Engels). Academic Press. p. 348. ISBN 9780080472072.
- ↑ "Mammalian inositol 3-phosphate synthase: its role in the biosynthesis of brain inositol and its clinical use as a psychoactive agent". Sub-cellular Biochemistry. 39: 293–314. 2006.
- ↑ Larner J (2002). "D-chiro-inositol--its functional role in insulin action and its deficit in insulin resistance". International Journal of Experimental Diabetes Research. 3 (1): 47–60. doi:10.1080/15604280212528. PMC 2478565. PMID 11900279.
- ↑ "Bile acids induce Ca2+ release from both the endoplasmic reticulum and acidic intracellular calcium stores through activation of inositol trisphosphate receptors and ryanodine receptors". The Journal of Biological Chemistry. 281 (52): 40154–63. 2006. doi:10.1074/jbc.M606402200.
- ↑ "Modulation of the kinetics of inositol 1,4,5-trisphosphate-induced [Ca2+]i oscillations by calcium entry in pituitary gonadotrophs". Biophysical Journal. 72 (2 Pt 1): 698–707. 1997. doi:10.1016/S0006-3495(97)78706-X.
- ↑ "G-proteins of fat-cells. Role in hormonal regulation of intracellular inositol 1,4,5-trisphosphate". The Biochemical Journal. 240 (1): 35–40. 1986.
- ↑ "Modulation of ATP-dependent chromatin-remodeling complexes by inositol polyphosphates". Science. 299 (5603): 112–4. 2003. doi:10.1126/science.1078068.
- ↑ "Regulation of chromatin remodeling by inositol polyphosphates". Science. 299 (5603): 114–6. 2003. doi:10.1126/science.1078062.
- ↑ 1937-, Mathews, Christopher K., (2000). Biochemistry. Van Holde, K. E. (Kensal Edward), 1928-, Ahern, Kevin G. (3rd uitg.). San Francisco, Calif.: Benjamin Cummings. p. 855. ISBN 0805330666. OCLC 42290721.
{{cite book}}: AS1-onderhoud: ekstra leestekens (link) AS1-onderhoud: meer as een naam (link) CS1 maint: numeric names: authors list (link) - ↑ Phytic acid
- ↑ Klopfenstein, Terry J. (Julie 2002). "Animal Diet Modification to Decrease the Potential for Nitrogen and Phosphorus Pollution". Council for Agricultural Science and Technology. 21.
- ↑ "Influence of vegetable protein sources on trace element and mineral bioavailability". The Journal of Nutrition. 133 (9): 2973S–7S. 2003.
- ↑ Committee on Food Protection (1973). "Phytates". Toxicants Occurring Naturally in Foods. National Academy of Sciences. pp. 363–371. ISBN 978-0-309-02117-3.
- ↑ Laurence, William L. "Corn by-product yields explosive", The New York Times. April 17, 1936. Page 7.
- ↑ Ledgard, Jared. The Preparatory Manual of Explosives, 2007. p. 366.
- ↑ "Inositol for depressive disorders". The Cochrane Database of Systematic Reviews (2): CD004049. 2004. doi:10.1002/14651858.CD004049.pub2.
- ↑ "Inositol in preterm infants at risk for or having respiratory distress syndrome". The Cochrane Database of Systematic Reviews (2): CD000366. 2015. doi:10.1002/14651858.CD000366.pub3.
- ↑ "Combining treatment with myo-inositol and D-chiro-inositol (40:1) is effective in restoring ovary function and metabolic balance in PCOS patients". Gynecological Endocrinology. 33 (1): 1–9. 2017. doi:10.1080/09513590.2016.1247797.
- ↑ "The combined therapy with myo-inositol and D-chiro-inositol reduces the risk of metabolic disease in PCOS overweight patients compared to myo-inositol supplementation alone". European Review for Medical and Pharmacological Sciences. 16 (5): 575–81. 2012.
- ↑ "argiefkopie". Geargiveer vanaf die oorspronklike op 8 September 2014. Besoek op 2 Oktober 2017.
- ↑ https://www.wired.com/underwire/2012/05/pl_drugs/.
- ↑ "Myo-inositol content of common foods: development of a high-myo-inositol diet". The American Journal of Clinical Nutrition. 33 (9): 1954–67. 1980.
