Aromatisiteit (chemie)
In die chemie is aromatisiteit 'n eienskap van sikliese (ringvormige), plat strukture met pi-bindings in resonansie (diegene wat gedelokaliseerde elektrone bevat) wat verhoogde stabiliteit verleen in vergelyking met ander geometriese of verbindingsrangskikkings met dieselfde stel atome. Aromatiese ringe is baie stabiel en breek nie maklik uitmekaar nie. Organiese verbindings wat nie aromaties is nie, word as alifatiese verbindings geklassifiseer. Sulke verbindings kan ringstrukture insluit, maar slegs aromatiese ringe het beter stabiliteit.
Aangesien die mees algemene aromatiese verbindings afgeleides van benseen is ('n aromatiese koolwaterstof wat algemeen voorkom in petroleum en die distillate daarvan), word die woord "aromaties" soms informeel gebruik na benseenderivate, en dit is dus was so die eerste keer gedefinieer. Nietemin bestaan daar baie nie-benseen aromatiese verbindings. In lewende organismes, byvoorbeeld, is die mees algemene aromatiese ringe die dubbelringbasisse in RNS en DNS. 'n Aromatiese funksionele groep of ander substituent word 'n arielgroep genoem.

Die vroegste gebruik van die term aromaties was in 'n artikel deur die Duitse chemikus August Wilhelm von Hofmann in 1855.[1] Hofmann het die term gebruik vir 'n klas benseenverbindings, waarvan baie reuke (aromas) het, in teenstelling met suiwer versadigde koolwaterstowwe. Aromatisiteit as 'n chemiese eienskap hou geen algemene verband met die reukeienskappe van sulke verbindings nie, hoewel chemici soos Hofmann in 1855, voordat die struktuur van benseen of organiese verbindings verstaan is, begin verstaan het dat geurige molekules van plante, soos terpeen, chemiese eienskappe het wat ons vandag herken en is soortgelyk aan onversadigde petroleumkoolwaterstowwe soos benseen.
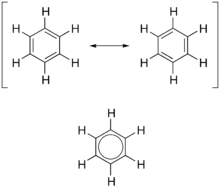
In terme van die elektroniese aard van die molekule, beskryf aromatisiteit 'n gekonjugeerde stelsel wat dikwels gemaak word van afwisselende enkel- en dubbelbindings in 'n ring. Hierdie konfigurasie laat toe dat die elektrone in die molekule se pi-stelsel om die ring gedelokaliseer word, wat die molekule se stabiliteit verhoog. Die molekuul kan nie deur een struktuur voorgestel word nie, maar eerder 'n resonansiebaster van verskillende strukture, soos met die twee resonansiestrukture van benseen. Hierdie molekules kan nie in een van hierdie voorstellings gevind word nie, met die langer enkelbande op een plek en die korter dubbele binding op 'n ander plek. Die molekuul vertoon eerder bindingslengtes tussen die van enkel- en dubbelbindings.
Hierdie model van aromatiese ringe, naamlik die idee dat benseen gevorm is uit 'n ses-ledige koolstofring met afwisselende enkel- en dubbelbindings (sikloheksatrien), is ontwikkel deur die Duitse organiese chemikus August Kekulé. Die model vir benseen bestaan uit twee resonansievorme, wat ooreenstem met die dubbel- en enkelbinding wat bo-op mekaar is om ses een-en-'n-half-bindings te produseer. Benseen is 'n meer stabiele molekuul as wat verwag sou word sonder om die ladingdelokalisering in ag te neem.
Variasies
[wysig | wysig bron]Aromatiese verbindings is belangrik in die industrie en word onttrek uit komplekse mengsels wat verkry word deur die raffinering van olie of deur distillasie van steenkoolteer, en word gebruik om 'n reeks belangrike chemikalieë en polimere te vervaardig, insluitend stireen, fenol, poliëster en nylon. 'n Groot aantal industriële toepassings behels heterosikliese aromatiese verbindings.
Heterosikliese aromatiese verbindinds
[wysig | wysig bron]
In heterosikliese aromatiese verbindings is een of meer atome in die aromatiese ring van 'n ander element as koolstof. Dit kan die aromatiteit van die ring verminder en sodoende die reaktiwiteit daarvan verhoog. Voorbeelde sluit in furaan, piridien, pirrool, imidasool, en tiofeen.
In hierdie voorbeelde is die aantal π-elektrone 6 as gevolg van die π-elektrone van die dubbelbindings sowel as die twee elektrone van enige enkele paar in die p-orbitaal wat in die vlak van die aromatiese π stelsel is. Byvoorbeeld, in piridien het die vyf sp2-gehibridiseerde koolstowwe elk 'n p-baan wat loodreg op die vlak van die ring is, en elkeen van hierdie p-orbitale bevat een π-elektron. Daarbenewens is die stikstofatoom ook sp2-gehybridiseer en het dit een elektron in 'n p-orbitaal, wat in totaal 6 p-elektrone maak, wat piridien aromaties maak. Die alleenstaande stikstof is nie deel van die aromatiese π-stelsel nie.
Pirrol en imidasool is albei vyfledige aromatiese ringe wat heteroatome bevat. In pirrool dra elk van die vier sp2-gehibrideerde koolstowwe een π-elektron by, en die stikstofatoom word ook sp2-gehybridiseer en dra twee π-elektrone by uit sy enkele paar, wat 'n p-orbitaal inneem. In imidasool word albei stikstofe sp2-gehibrideer; die een in die dubbelbinding dra een elektron by en die een wat nie in die dubbelbinding is nie en in 'n alleenpaar is, dra twee elektrone by tot die π-stelsel.[2]
Gesmelte aromatiese en polisikliese stowwe
[wysig | wysig bron]
Polisikliese aromatiese koolwaterstowwe is molekules wat twee of meer eenvoudige aromatiese ringe bevat wat saamgesmelt word deur twee naburige koolstofatome te deel. Voorbeelde hiervan is naftaleen, antraseen en fenantreen. In versmelte aromatiese stowwe is nie alle koolstof-koolstofbindings noodwendig ekwivalent nie, aangesien die elektrone nie oor die hele molekule gedelokaliseer word nie. Die aromatiteit van hierdie molekules kan aan die hand van hul orbitale prentjie verklaar word. Soos benseen en ander monosikliese aromatiese molekules, het polisikliese 'n sikliese gekonjugeerde 'n pi-elektronstelsel met p-orbitale oorvleueling bo en onder die vlak van die ring.[2]
Een ongewone aanwending van antrasene is in gloeistokkies.
Vervangde aromatiese verbindings
[wysig | wysig bron]Baie chemiese verbindings is aromatiese ringe met ander funksionele groepe aangeheg. Voorbeelde sluit in trinitrotolueen (TNT), asetielsalisielsuur (aspirien), parasetamol en die nukleotiede van DNS.
Verwysings
[wysig | wysig bron]- ↑ Hofmann, A. W. (1855). "On Insolinic Acid". Proceedings of the Royal Society (in Engels). 8: 1–3. doi:10.1098/rspl.1856.0002.
- ↑ 2,0 2,1 McMurry, John (2011). Organic Chemistry (in Engels) (8de uitg.). Brooks-Cole. p. 544. ISBN 978-0-8400-5444-9.
