Organiese nomenklatuur
In organiese chemie is die organiese nomenklatuur 'n metode om organiese chemiese verbindings name te gee soos aanbeveel deur die Internasionale Unie van Suiwer en Toegepaste Chemie (IUSTC).[1] Ideaal gesproke moet elke moontlike organiese verbinding 'n naam hê waarvan 'n ondubbelsinnige struktuurformule geskep kan word. Daar is ook 'n lys IUSTC-benoemingsaanbevelings vir anorganiese chemie.
Om lang en vervelige name in normale kommunikasie te vermy, word die amptelike IUSTC-benoemingsaanbevelings nie altyd in die praktyk gevolg nie, behalwe as dit nodig is om 'n eenduidige en absolute definisie aan 'n verbinding te gee. IUSTC-name kan soms eenvoudiger wees as ouer name, soos met etanol, in plaas van etielalkohol of cholesterol wat makliker is as die sistematiese naam (3S,8S,9S,10R,13R,14S,17R)-10,13-dimetiel-17-[(2R)-6-metielheptaan-2-iel]-2,3,4,7,8,9,11,12,14,15,16,17-dodekahidro-1H-siklopenta[a]fenantren-3-ol.[2]
Vir relatief eenvoudige molekules is dit makliker om die nie-sistematiese name te verstaan, wat geleer of na gekyk moet word. Die algemene of triviale naam is egter dikwels aansienlik korter en duideliker, en dit word dus verkies. Hierdie nie-sistematiese name is dikwels afgelei van die oorspronklike bron van die verbinding. Daarbenewens kan baie lang name minder duidelik wees as die struktuurformule. Die sistematiese naam maak dit nogtans moontlik om die hele molekuulstruktuur af te lei.
Die bekendste organiese stowwe het name in die omgangstaal, of daar word ouer name uit die geskiedenis van die chemie gebruik, maar dersuisende verbindings het geen naam in die omgangstaal nie.
Beginsels vir koolwaterstofkettings
[wysig | wysig bron]Alkane
[wysig | wysig bron]- Hoofartikel: Alkaan
Reguit-ketting alkane neem die agtervoegsel "-aan" en kry die voorvoorvoegsel afhangende van die aantal koolstofatome in die ketting, volgens standaardreëls. Die eerste paar voorvoegsels is:
| Antal koolstofatome | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Voorvoegsel | Met | Et | Prop | But | Pent | Heks | Hept | Okt | Non | Dec | Undek | Dodek | Tridek | Tetradek | Pentadek | Heksadek | Heptadek | Oktadek | Nonadek | Ikos |
Byvoorbeeld, die eenvoudigste alkaan is CH4 (metaan) en die negekoolstof-alkaan CH3(CH2)7CH3 word nonaan genoem. Die name van die eerste vier alkane is onderskeidelik afgelei van metanol, eter, propionsuur en "bottersuur" (butanoësuur). Die res word met 'n Griekse numeriese voorvoegsel benoem, met die uitsondering van nonane met 'n Latynse voorvoegsel, en undekaan en tridekaan met voorvoegsels uit gemengde tale.
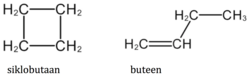
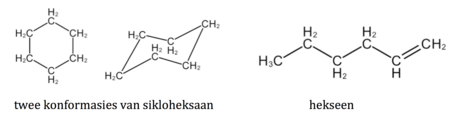
Sikliese alkane kry eenvoudig die voorvoegsel "siklo-", bv. C4H8 is siklobutaan (nie te verwar met buteen nie) en C6H12 is sikloheksaan (wat nie met hekseen verwar moet word nie).

Vertakte alkane word die naam van 'n reguit ketting-alkaan gegee met aangehegde alkielgroepe. 'n Nommer voor die naam word gebruik on die koolstofatoom aan te dui waaraan die groep geheg is, en word getel vanaf die einde van die alkaanketting. Byvoorbeeld, (CH3)2CHCH3, algemeen bekend as isobutaan, word beskryf as 'n propaanketting met 'n metielgroep wat aan die middelste (nommer 2) koolstof gebind is, en die sistematiese naam 2-metielpropaan kry. Alhoewel die naam 2-metielpropaan gebruik kan word, is dit makliker en logieser om dit bloot metielpropaan te noem - die metielgroep kan onmoontlik op enige van die ander koolstofatome voorkom (wat die ketting sal verleng en butaan vorm, en nie propaan nie) en daarom is die gebruik van die nommer "2" onnodig.

As daar 'n onduidelikheid in die posisie van die syketting is, afhangend van die punt van die alkaanketting begin getel word, word die nommering gekies sodat die kleiner getal gebruik word. Byvoorbeeld (CH3)2CHCH2CH3 (isopentaan) word 2-metielbutaan genoem, nie 3-metielbutaan nie.
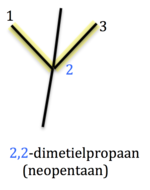
As daar meervoudige sytakke van dieselfde groote alkielgroep is, word hulle posisies deur komma's geskei en die groep word voorafgegaan deur di-, tri-, tetra-, ens. afhangende van die aantal takke. Byvoorbeeld, C(CH3)4 (neopentaan) word 2,2-dimetielpropaan genoem.

As daar verskillende groepe is, word hulle in alfabetiese volgorde bygevoeg, geskei deur komma's of koppeltekens. Die langste moontlike hoof-alkaanketting word gebruik; dus 3-etiel-4-metielheksaan in plaas van 2,3-diëtielpentaan, al beskryf dit ekwivalente strukture.
Die voorvoegsels di-, tri- ens. word geïgnoreer vir die doel van alfabetiese ordening van sykettings (bv. 3-etiel-2,4-dimetielpentaan, nie 2,4-dimetiel-3-etielpentaan nie).
Alkene
[wysig | wysig bron]- Hoofartikel: Alkeen
Alkenes is vernoem na hul ouer-alkaanketting met die agtervoegsel "-een" en 'n vaste nommer wat die posisie van die koolstof aandui met die laagste getal vir elke dubbelbinding in die ketting: CH2=CHCH2CH3 is but-1-een.
Meervoudige dubbele bindings het die vorm-diëen, -triëen, ens. en die voorvoegsel van die ketting wat die groote aandui neem 'n ekstra "a": CH2=CHCH=CH2 is buta-1,3-dieen.
Eenvoudige cis- en trans-isomere kan aangedui word met 'n voorvoegsel cis- of trans-: cis-but-2-een, trans-but-2-een. Cis- en trans- is egter relatiewe beskrywers. Dit is die IUSTC-konvensie om alle alkene te beskryf met behulp van absolute beskrywers van Z-(dieselfde kant) en E-(teenoorgestelde) met behulp van die Cahn–Ingold–Prelog-prioriteitsreëls.[3][4]
Alkyne
[wysig | wysig bron]- Hoofartikel: Alkyn

Alkyne gebruik die selfde reëls maar eindig met die agtervoegsel "yn", bv. etyn (asetileen) en propyn (metielasetileen).
Beginsels vir funksionele groepe
[wysig | wysig bron]- Hoofartikel: Funksionele groep
Halogenoalkane en Halogenoarene
[wysig | wysig bron]- Hoofartikels: Halogenoalkaan en Halogenoareen

In halogenoalkane en halogenoarene word die funksionele halogeengroepe voorafgegaan met die bindingsposisie en neem die vorm aan van fluor-, chloor-, broom-, jood-, ens., afhangende van die halogeen. Veelvuldige groepe is dichloro-, trichloro-, ens., en verskillende groepe word soos voorheen alfabeties georde. CHCl3 (chloroform) is byvoorbeeld trichloormetaan. Die verdowingsmiddel Halotaan (CF3CHBrCl) is 2-broom-2-chloor-1,1,1-trifluoroetaan.
Alkohol
[wysig | wysig bron]- Hoofartikel: Alkohol
Alkohols (R-OH) neem die agtervoegsel "-ol" met 'n invoegsel van die numeriese bindingsposisie: bv. CH3CH2CH2OH is propaan-1-ol. Die agtervoegsels -diol, -triol, -tetraol, ens., word gebruik vir veelvuldige -OH-groepe: Etileenglikol CH2OHCH2OH is etaan-1,2-diol.
As 'n funksionele groep met 'n hoër voorrang in die molekule voorkom, word die voorvoegsel "hidroksi" met die bindingsposisie gebruik. bv. CH3CHOHCOOH is 2-hidroksipropanoësuur.
Eters
[wysig | wysig bron]- Hoofartikel: Eter
Eters (R-O-R) bestaan uit 'n suurstofatoom tussen die twee aangehegte koolstofkettings. Die korter van die twee kettings word die eerste deel van die naam met die "-aan" agtervoegsel verander na "-oksi", en die langer alkaanketting word die agtervoegsel van die naam van die eter. Dus is CH3OCH3 metoksimetaan, en CH3OCH2CH3 is metoksi-etaan, en nie etoksimetaan nie. As die suurstof nie aan die einde van die hoof-alkaanketting geheg word nie, word die hele korter alkiel-plus-etergroep as 'n sy-ketting behandel en voorafgegaan met sy bindingsposisie op die hoofketting. Dus is CH3OCH(CH3)2 2-metoksipropaan.
Alternatiewelik kan 'n eterketting genoem word as 'n alkaan waarin een koolstof deur 'n suurstof vervang word, 'n vervanging aangedui deur die voorvoegsel 'oksa'. CH3OCH2CH3 kan byvoorbeeld ook 2-oksabutaan genoem word, en 'n epoksied ('n sikliese eter met 'n drie-atoomring) kan oksasiklopropaan genoem word. Hierdie metode is veral handig wanneer beide groepe wat aan die suurstofatoom geheg is, kompleks is.[5]
Amiene
[wysig | wysig bron]- Hoofartikel: Amien
Amiene (R-NH2) is vernoem na die aangehegte alkaanketting met die agtervoegsel "-amien" (bv. CH3NH2 metaanamien). Indien nodig, word die bindingsposisie ingevoeg: CH3CH2CH2NH2 propaan-1-amien, CH3CHNH2CH3 propaan-2-amien. Die voorvoegselvorm is "amieno-".
Vir sekondêre amiene (met die vorm R-NH-R) is die primêre naam van die amien die langste koolstofketting wat aan die stikstofatoom geheg is. Die ander ketting is voorgevoeg as 'n alkielgroep met die posisievoorvoegsel 'n skuinskrif N: CH3NHCH2CH3 is N-metieletaanamien. Tersiêre amiene (R-NR-R) word soortgelyk behandel: CH3CH2N(CH3)CH2CH2CH3 is N-etiel-N-metielpropaanamien. Weereens word die substituentgroepe alfabeties gerangskik.
Amiede
[wysig | wysig bron]- Hoofartikel: Amied
Amiede (R-CO-NH2) neem die agtervoegsel "-amied" of "-karboksamied" wanneer die koolstof in die amiedgroep nie in die hoofketting opgeneem kan word nie. Die voorvoegselvorm is beide "karbomiel-" en "amiedo-". Byvoorbeeld HCONH2 Metaanamied, CH3CONH2 Etaanamied.
Amiede wat addisionele substituente op die stikstof bevat, word soortgelyk aan die geval van amiene behandel: hulle word alfabeties gerangskik met die voorvoegsel N: HCON(CH3)2 is N,N-dimetielmetaanamied.
Opsomming van basiese beginsels en voorbeeld
[wysig | wysig bron]In die chemie word 'n aantal voorvoegsels, agtervoegsels en invoegsels gebruik om die tipe en posisie van die funksionele groepe in die verbinding te beskryf.
Die stappe vir die benaming van 'n organiese verbinding is:
- Identifisering van die moederkoolwaterstofketting. Hierdie ketting moet die volgende reëls in volgorder nakom:
- Dit moet die maksimum aantal substituente of takke hê wat as voorvoegsels aangehaal word
- Dit moet die maksimum aantal substituente van die agtervoegsel funksionele groep bevat. (Met agtervoegsel word bedoel dat die ouerfunksionele groep 'n agtervoegsel moet hê, anders as halogeen-substituente). As meer as een funksionele groep teenwoordig is, moet die groep met die hoogste voorrang gebruik word.
- Dit moet die maksimum lengte hê.
- Dit moet die maksimum aantal veelvuldige verbindings hê.
- Dit moet die maksimum aantal enkelverbindings hê.
- Identifikasie van die ouerfunksionele groep, indien enige, met die hoogste prioriteit.
- Identifisering van die sykettings. Kantkettings is die koolstofkettings wat nie in die moederketting is nie, maar daarvan vertak.
- Identifisering van die oorblywende funksionele groepe en benoem dit aan die hand van hul ioniese voorvoegsels (soos hidroksie vir -OH, oksie vir = O, oksie-alkaan vir O-R, ens.).
Verskillende sykettings en funksionele groepe sal in alfabetiese volgorde saamgevoeg word. (Die voorvoegsels di-, tri-, ens. word nie in ag geneem vir alfabetiese groepering nie. Byvoorbeeld, etiel kom voor dihiedroksie of dimetiel, aangesien die "di" word in geen geval oorweeg word nie). Wanneer beide sykettings en sekondêre funksionele groepe teenwoordig is, moet dit in een groep gemeng word, eerder as in twee afsonderlike groepe. - Identifisering van dubbel- en drievoudige bindings.
- Nommer van die ketting. Dit word gedoen deur eers die ketting in beide rigtings te nommer (links na regs en regs na links), en dan die nommerorder wat volgens die reëls wat volg te kies, in die voorrangorde:
- Dit het die laagste nommer (of lokant) vir die agtervoegsel funksionele groep. Lokante is die nommers op die koolstowwe waaraan die substituente direk geheg is.
- Dit het die lokante vir veelvoudige bindings met die laagste nommer (Die lokant van 'n veelvoudige binding is die nommer van die aangrensende koolstof met 'n laer getal).
- Dit het die laagste nommer vir die voorvoegsels.
- Nommer van die verskillende substituente en verbindings met hul lokante. As daar meer as een van dieselfde tipe substituent / dubbelbinding is, word 'n voorvoegsel bygevoeg wat wys hoeveel daar is (di - 2, tri - 3, tetra - 4, net soos vir die aantal koolstowwe hieronder met 'a' bygevoeg)
Die getalle vir dié tipe syketting word in stygende volgorde gegroepeer en voor die naam van die syketting geskryf. As daar twee sykettings met dieselfde alfakoolstof is, sal die getal twee keer geskryf word. Voorbeeld: 2,2,3-trimetiel-. As daar beide dubbel- en drievoudige bindings is, word "een" (dubbelband) voor "yn" (drievoudige binding) geskryf. Wanneer die hooffunksionele groep 'n terminale funksionele groep is ('n groep wat slegs aan die einde van 'n ketting kan bestaan, soos formiel- en karboksielgroepe), hoef dit nie 'n nommer te kry nie.
- Rangskikking in hierdie vorm: Samegroeping van die sykettings en sekondêre funksionele groepe met getalle vanaf stap 3 + voorvoegsel van ouer koolwaterstofketting (et-, met-) + dubbel / drievoudige bindings met getalle (of "aan") + primêre funksionele groepvoorvoegsel met getalle.
Waar daar ook "met getalle" staan, word verstaan dat tussen die woord en die getalle die voorvoegsel (di-, tri-) gebruik word. - Byvoeging van leestekens:
- Kommas word tussen getalle geplaas (2 5 5 word 2,5,5)
- Koppeltekens word tussen 'n nommer en 'n letter geplaas (2,5,5 trimetylheptaan word 2,5,5-trimetielheptaan)
- Opeenvolgende woorde word in een woord saamgevoeg (trimetiel heptaan word trimetielheptaan)
Opmerking: IUSTC gebruik deurgaans eenwoordname. Dit is die rede waarom alle onderdele verbind is.
Voorbeeld van 'n molekule met die moederkoolstowwe genommer 1 tot 23, en die ander atoome (behalwe waterstof) ook genommer:

Volg nou die bogenoemde stappe:
- Die moederkoolwaterstofketting het 23 koolstowwe. Dit word trikosa- genoem.
- Die funksionele groepe met die hoogste voorrang is die twee ketoongroepe (nommers 24 en 25).
- Die groepe is op koolstofatome 3 en 9. Aangesien daar twee is, skryf ons 3,9-dioon.
- Die nommering van die molekule is gebaseer op die ketoongroepe. As ons van links na regs nommer is die ketoongroepe nommers 3 en 9. Wanneer ons van regs na links nommer, is die ketoongroepe nommers 15 en 21. 3 is minder as 15, daarom is die ketone 3 en 9. Die kleiner nommers word altyd gebruik.
- Die sykettings is: 'n etiel- aan koolstof 4, etiel- aan koolstof 8 en 'n butiel- aan koolstof 12.
Opmerking: Die -O-CH3 aan koolstofatoom 15 is nie 'n syketting nie, maar wel 'n metoksie funksionele groep.- Daar is twee etielgroepe. Hulle word gekombineer om 4,8-diëtiel te skep.
- Die sykettings is so gegroepeer: 12-butiel-4,8-diëtiel. (Maar dit is nie noodwendig die finale groepering nie, want daar kan tussentyd funksionele groepe bygevoeg word om te verseker dat alle groepe alfabeties gelys word.)
- Die sekondêre funksionele groepe is: 'n hidroksie- aan koolstof 5, 'n chloor- aan koolstof 11, 'n metoksie- aan koolstof 15 en 'n broom- aan koolstof 18. Gegroepeer met die sykettings gee dit 18-broom-12-butiel-11-chloor-4,8-diëtiel-5-hidroksie-15-metoksie.
- Daar is twee dubbele verbindings: een tussen koolstof 6 en 7, en een tussen koolstof 13 en 14 en dit sal 6,13-dieen genoem word. Daar is een drievoudige verbinding tussen koolstofatome 19 en 20. Dit word 19-yn genoem.
- Die rangskikking (met leestekens) is: 18-broom-12-butiel-11-chloor-4,8-diëtiel-5-hidroksie-15-metoksietrikosa-6,13-dieen-19-yn-3,9-dioon
- Ten slotte, as gevolg van die moontlike cis-trans-isomere, moet ons die relatiewe oriëntasie van funksionele groepe rondom elke dubbelbinding spesifiseer. Vir hierdie voorbeeld het ons (6E,13E)
Die finale naam is dus:
(6E,13E)-18-broom-12-butiel-11-chloor-4,8-diëtiel-5-hidroksie-15-metoksietrikosa-6,13-dieen-19-yn-3,9-dioon.
Kyk ook
[wysig | wysig bron]Verwysings
[wysig | wysig bron]- ↑ The Commission on the Nomenclature of Organic Chemistry (1971) [1958 (A: Hydrocarbons, and B: Fundamental Heterocyclic Systems), 1965 (C: Characteristic Groups)]. Nomenclature of Organic Chemistry (in Engels) (3de uitg.). London: Butterworths. ISBN 0-408-70144-7.
- ↑ PubChem. "Cholesterol". PubChem (in Engels). Besoek op 6 Oktober 2020.
- ↑ March, Jerry; Smith, Michael B. (2007). March's advanced organic chemistry : reactions, mechanisms, and structure (in Engels) (6 uitg.). Hoboken, NJ: Wiley-Interscience. ISBN 978-0-471-72091-1. OCLC 69020965.
- ↑ Cross, L.C; Klyne, W. (1974). Rules for the Nomenclature of Organic Chemistry: Section E: Stereochemistry (Recommendations 1974) (PDF) (in Engels). ISBN 978-0-08-021019-3. Geargiveer vanaf die oorspronklike (PDF) op 7 April 2016.
- ↑ Hunt, Ian R. "Ethers". Chemistry (in Engels). Besoek op 8 Oktober 2020.